「人を対象とする生命科学・医学系研究」の 説明文書
手順書様式2
「人を対象とする生命科学・医学系研究」の 説明文書
熊本大学および共同研究機関では、生命科学・医学系研究に協力してくださる方々(以下、研究対象者)の利益と安全を守り、安心して研究に参加していただくように心がけています。生命科学・医学系研究を実施する場合は、事前に、担当の研究者もしくは医療者が研究内容を十分に説明し、その主旨を研究対象者になっていただく皆さまにしっかりと理解していただくように心がけています。説明を聞かれ、研究参加に同意される場合は、同意書に署名をして、担当の研究者もしくは医療者にお返しください。
なお、研究対象者になっていただく皆さまには、生命科学・医学系研究の実施に同意しない権利も保障されています。同意されなくても、また一旦出された同意を撤回されても不利益を受けることは一切ありません。
また、当該の研究計画は熊本大学大学院生命科学研究部等「人を対象とする生命科学・医学系研究」倫理委員会(疫学・一般研究部門/臨床研究部門)で審査され、その承認を受け、熊本大学大学院生命科学研究部長/熊本大学病院長の許可を受けています。
| 研究の名称:成人発症免疫不全症の疾患レジストリ・検体レポジトリの構築と前向き観察研究 |
説明内容
1.研究の目的:
播種性非結核性抗酸菌症を発症した症例で血中インターフェロンγ抗体を測定することで、成人発症免疫不全症(AOID)を抽出し、診療実態の把握として、特定の時期に多くの患者さんの情報を集めて分析・調査し、疾患基盤情報を集める。同時に疾患レジストリ(病気の情報を集めたデータベース)を構築し前向きコホート研究(臨床経過の推移を5年間にわたり収集)を行い、同疾患の自然経過、予後を解析します。
本計画により整備された疾患基盤情報に基づき適正な診療指針の策定を試みると同時に、検体レポジトリ(患者さんの検体(血液や組織など)を保管する仕組み)を用いた疾患機序の解明にむけた基礎検討の礎とすることを目指します。
2.方法の概略:
2-1. 研究の方法(研究対象者から取得された試料・情報の利用目的を含む。)
熊本大学呼吸器内科で抗IFN-γ自己抗体の測定を行い、成人発症免疫不全症の診断を確定した後に1年に1 回定期的な経過観察・検査を行っていきます。
本研究への参加同意をいただいた日から診療に合わせて1年に1回の定期観察と検査を行っていきます。定期検査では1年に1回、身体診察、問診、血液検査を行い、下記の項目の情報を収集いたします。また、病状に応じて主治医の判断で胸部単純X線写真、CT、MRIなどの画像検査を行います。また、本研究に参加することで追加となる項目としては、20mlの研究用採血となります。この病気の病因といわれている抗IFN-γ自己抗体の推移を測定するため、また、病因を解析する(遺伝子解析を含む)ために追加採血・保存を行います。追加研究および遺伝子解析を行う際には改めて倫理申請を行い、対象者への情報提供、同意書を取得する可能性があります。
【登録時臨床項目】
性別、生年月日、身長、体重、BMI、職業、喫煙歴、出産歴、出生国、居住市町村、感染症の有無、併存症(糖尿病、透析、血液疾患、悪性腫瘍、リンパ腫、その他)、免疫不全をもたらす薬物療法(ステロイド・免疫抑制剤、バイオ製剤、抗癌剤、その他)、家族歴、播種性NTM症経過(症状、皮膚病変、治療内容、罹患臓器、NTM検出臓器、治療内容)、病変評価モダリティ(CT、MRI、Gaシンチ、PET-CT)、血液検査所見、抗IFN-γ抗体の有無(濃度・中和能)
【各Visitにおける観察項目】
治療と経過状況
・症状
・皮膚病変(前回からの変化の有無)
・感染症
・治療内容(抗菌薬の変更・中止)
・転帰(主治医判断による改善・不変・増悪、死亡、死因(自由記載)、中止した場合の再燃の有無、再燃臓器、画像の転帰)
・画像情報(CT、MRI、Gaシンチ、PET-CT)
・血液検査
・抗IFNγ抗体の有無(濃度・中和能)
【検査項目】
1)一般臨床検査は、以下の項目を測定する。
血算(白血球数、白血球分画)
血液生化学:TP,Alb, HbA1c, CRP, Ca, T-SPOT, QFT, 抗MAC抗体)
抗IFN-γ抗体
2)研究用特殊血液検査(DNA、RNAおよび血清・血漿および末梢血単核球(PBMC)保存)
本研究は、全国に所在する計32施設の共同研究として実施されます。
本研究によってえられた検体・情報は、個人が特定されないように匿名化したうえで、解析は熊本大学、慶應義塾大学で保存・解析を行います。
本研究は、人を対象とする生命科学・医学系研究に関する倫理指針(文部科学省・厚生労働省告示令和5年3月27日)およびヘルシンキ宣言(2013年改訂)を遵守して実施します。
2-2. 研究の期間
予定研究期間は、2025年の倫理委員会での承認日~2032年3月31日まで5年間の経過を観察します。
研究のスケジュール
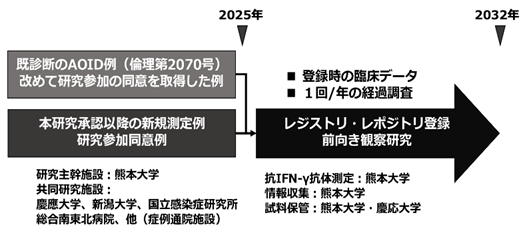
*コホートA:先行研究(倫理2070号)で登録されたAOIDと診断された方
*コホートB:2024年度以降に熊本大学呼吸器内科で抗IFN-γ自己抗体の測定を行いAOIDと診断された方
来院のスケジュールについて:
原則として、同意取得の日を基準として少なくとも1年毎の来院(前後6か月以内)の来院をお願いします。
2-3. 研究対象者として選定された理由
【研究に参加していただける方の主な条件】
① 先行研究(倫理2070号)で登録されたAOIDと診断された方
② 2024年度以降に熊本大学呼吸器内科で抗IFN-γ自己抗体の測定を行いAOIDと診断された方
③ 同意取得時において、年齢が18歳以上の方:本研究への参加にあたり説明を十分に理解し、ご自身の意思で同意書に署名できる方
【研究に参加していただけない方の主な条件】
① 成人症例を対象とするために18歳未満の方
② そのほか担当医師が不適当と判断した方
【研究への参加を中止する場合】
この研究への参加をされたあとでも、下記のように研究への参加を中止することがあります。あなたの意思に反して中止せざるを得ない場合もありますが、あらかじめご了承ください。中止する場合には、その理由およびそれまでのデータの活用方法などを担当医師からご説明いたします。また、中止後も担当医師が誠意をもってあなたの治療にあたりますので、ご安心ください。
① 患者様から研究への参加の中止を希望された場合
② 病気の状態や経過などから、担当医師が研究を中止したほうがよいと判断した場合
③ この臨床研究全体が中止となった場合
④ そのほか、担当医師が中止したほうがよいと判断した場合
3.研究参加によって得られる利益:
成人発症免疫不全症の疾患基盤情報に基づき適正な診療指針が策定できれば、より効果的な診療を行うことができます。また、検体レポジトリを用いた疾患機序の解明にむけた基礎検討の礎となり、最適な治療が見つかる可能性があります。そうすれば、将来的に治療方法が改善し、利益を受ける可能性があります。また、同じ病気の患者さんに貢献できる可能性があります。
4.研究によって生じる負担、危険性及び合併症(妊婦又は妊娠する可能性のある研究対象者についての胎児についての情報も含むこと。)
この研究にご参加いただく場合には、通常診療を超える検査として、研究用採血(全血で1年に1回20ml)をさせていただきます。採血については、通常の採血と同様に静脈からの採血を行います。この量は、患者様のお身体にとって医学的に問題のない量と考えております。
なお、研究の参加中に何らかのお身体の不調や気になる症状がありましたら、担当医師にお知らせください。必要に応じて、適切なアドバイスを行います。その結果、担当医師の判断により、検査を追加したり、場合によっては研究を中止したりすることもあります。
5.代替手段とその期待しうる効果、危険性及び合併症
成人発症免疫不全症は希少疾患であり、臨床的背景と診療実態は明らかになっていません。これまでも、症例報告での知見集積しかなくガイドラインの策定も行われていないことから、実地臨床においては経験的な診療が各症例に行われているのが実情です。本観察研究に参加中でも、担当医が必要と認めた追加治療は行うことができますが、追加治療の情報も収集の対象となります。それらの情報の収集により、本疾患の病態解明に繋がります。
本研究は、観察研究であり、この研究に参加しない場合でも、通常診療が行われます。
6.この研究に参加しない場合:
この研究に参加しない場合でも、通常診療での治療をうけることが可能です。研究への参加をお断りになられたとしても、今後の診療に影響することはありません。
7.その他:
7-1. 研究対象者に生じる経済的負担と謝礼
この研究は、通常診療の範囲内で行われますので、検査費用については、保険診療を適応した分の患者様の経済的な負担が発生します。ただし、研究用採血にかかる保険診療適応外の検査に関しては、研究組織で負担をしますので、追加でのご負担が発生することはありません。また、この研究では研究参加に対しての謝礼はございません。
7-2. 同意の撤回について
この研究への参加に同意した場合であっても、患者様はいつでも同意を撤回していただくことができます。同意の撤回があってもその後の診療には影響や不利益が生じることはありません。
7-3. 研究に関する情報公開の方法
本研究は、UMIN(University Hospital Medical Information:大学病院医療情報ネットワーク)へ登録します。
7-4. 個人情報等の取扱いについて(匿名化する場合にはその方法を含む。)
個人情報は、研究のために特定した目的、項目に限り適正に取得、利用します。個人の特定につながる氏名、生年月日に関しては取得せず、参加者それぞれに番号を割り当てて対応表を作成することで匿名化を行います。取得した情報を用いて解析した研究の結果は、論文や学会発表として公表されますが、公表される情報には個人を特定しうる情報は含まれませんのでご安心ください。取得した情報は万全の管理対策を講じ、管理責任者である熊本大学呼吸器内科坂上拓郎が適切に保護し慎重に取り扱います。個人を特定できる情報が熊本大学から外部にでることはありません。
7-5. 試料・情報の保管及び廃棄の方法について
この研究により採取された調査結果や血液などの検体は、熊本大学病院呼吸器内科医局内の施錠ができる部屋で保管し、残った検体は一見して個人が特定できないように匿名化し、保管期間が終了した後に廃棄いたします。また、研究に関連する情報は研究終了後15年間の保存を行います。追加研究が必要になった場合には、随時倫理委員会に申請を行います。検体や情報を廃棄する場合は、個人を識別できない状態で適切に廃棄いたします。
7-6.研究対象者やその子孫の健康に関する研究結果のフィードバックについて
研究を行うなかで、想定していなかった患者様やご家族に重大な影響を与える結果が偶然に得られる場合があります。そのような結果について、説明をご希望される場合には、担当医師までご連絡ください。私共の倫理委員会と相談のうえ、対応させていただきます。また、参加者様及び代諾者等からの希望がない場合でも、生命の危機に関するような検査結果が得られた場合には、同様に倫理委員会に相談し、報告させていただくか検討します。
7-7. 利益相反について
利益相反とは、外部との経済的な利益関係等によって、研究データの改ざん、特定企業の優遇など研究が公正かつ適切に行われていないと第三者から懸念されかねない事態のことを指します。本研究において研究の公正さを損なうような利益相反はありません。本研究における利益相反に関する状況は、熊本大学大学院生命科学研究部等医学系研究利益相反委員会の審査を得ております。
7-8. 本研究によって生じた健康被害に関する対応・補償について
この研究においては、通常診療として、血液検査、胸部画像検査、呼吸機能検査、動脈血液ガスに関しては、保険診療の範囲内で行います。この研究に起因して健康被害が生じた場合も、通常の保険診療と同様に患者様の健康保険を用いて治療を行います。その際の医療費の自己負担分の支払い、休業補償、差額ベッド料金の補填などの金銭的な補償はいたしません。万が一健康被害が生じた場合は、保険診療の範囲内で適切に対応します。
7-9. いただいた試料・情報が将来の研究で使用される可能性
今回の研究参加によって得られた情報を将来の研究で利用(二次利用)する場合には、改めてその研究計画を適切な審査委員会において審査し、データ類の扱いも含め、適切な研究計画であるかどうか評価がなされて、必ず学長/院長の許可を得て、初めて実施されます。また、二次利用の内容について当院のホームページで情報を公開します。このような確認の過程を経ず、あなたに無断で二次利用されることはありません。
7-10. モニタリング・監査について
本研究は侵襲や介入を伴わない観察研究であり、モニタリング・監査については予定しておりません。
7-11. 本研究に対する問い合わせ先(24時間対応可能な連絡先)ならびに担当者
この研究について、何かお尋ねになりたいことや心配なことがありましたら以下の相談窓口連絡先までお問い合わせください。なお、本疾病に関する相談事は各担当医へご相談ください。
【相談窓口連絡先】
熊本大学病院呼吸器内科 坂田 晋也
TEL:096-373-5012
〒860-8556 熊本市中央区本荘1-1-1
なお、個人情報や研究者の知的財産権の保護等の観点から、すべての情報を開示できない場合がありますのでご了承ください。
臨床研究(オプトアウト)一覧へ





